
CCS(Contamination Control Strategy,污染控制策略)由欧盟无菌附录一修订后引入,近来随PDA TR90报告的颁布而被频频提出,制药人之前熟知的CCS(Container Closure System容器密封系统)有了另一种定义,新的CCS(污染控制策略)目的是什么?他们之间是否存在联系?本文将做针对生物制药中的CCS(污染控制策略,下文称为“新CCS”)进行简述,以供读者参考。
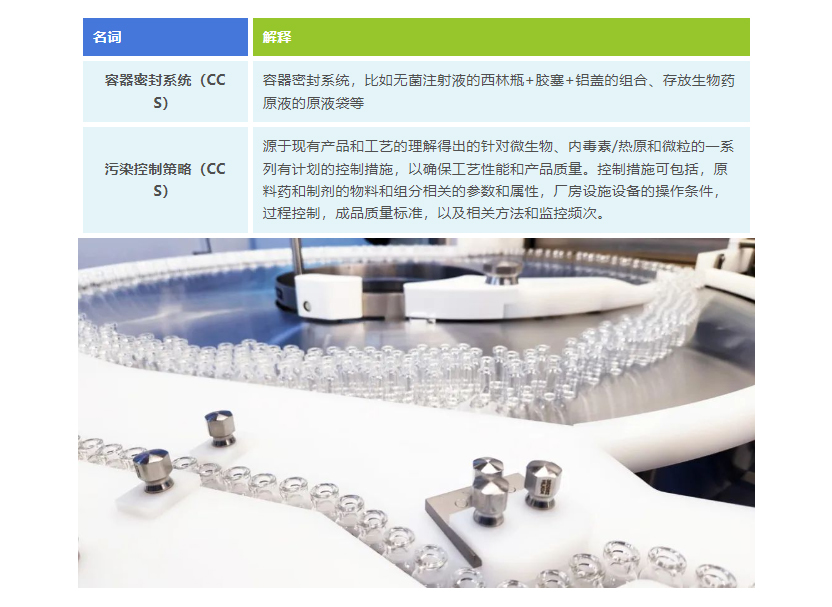
██ 名词解释
██ 新CCS提出的目的
各国药品生产质量管理规范(GMP)的提出均涉及一个共同的目标“最大限度地降低药品生产过程中污染、交叉污染以及混淆、差错等风险,确保持续稳定地生产出符合预定用途和注册要求的药品”。而为了满足这一目标,“污染控制措施”是一个核心要素,但各国GMP内列举的污染控制措施多为单独存在使用的,并无文件来明确各控制措施之间的相互依存关系。新CCS的提出,旨在将污染控制向着整体分析的方向转变,避免单独污染控制措施之间的风险疏漏或单独污染控制措施的过度执行,也可有效的推动持续改进和/或改正。

██ 新CCS的基本要素
污染控制策略是一个相互交织和连续关联的元素组合,包含了药品质量体系和GMP措施的许多要素,图一说明了这些要素的相互关系。
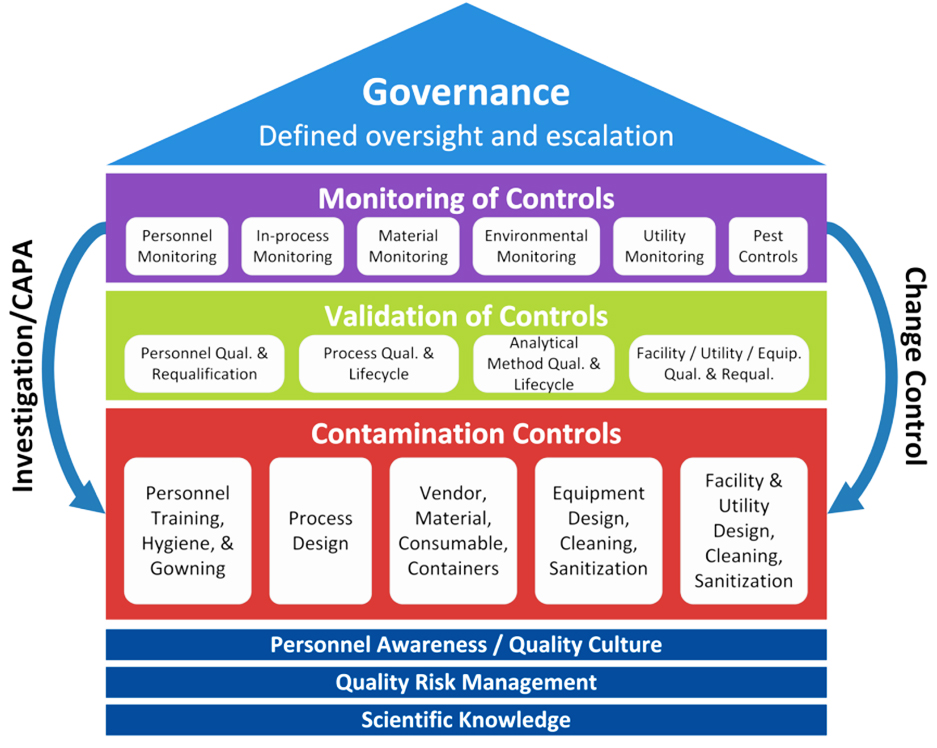
图一:Elements of a Contamination Control Strategy (courtesy of Sanofi)
如图所示,污染控制策略涵盖了人员培训、工艺设计、设备设计、公用工程设计、人员意识、质量风险管理、过程监控等各种要素。在开发/设计污染控制策略时,应尽量设计具有独立控制的要素,以避免单个要素失败而导致污染,比如生物制药中的制剂生产药液配制工序,如采用密闭系统转移药液,则无需担心环境及人员对药液产生影响。

██ 新CCS的应用举例
新CCS主要针对的是污染控制,其可以由单点展开开发(如特定设备、流程的CCS开发,多用于多产品、多类型产线)后互相引用支持、也可以按照产品生产工艺将所有项目穿插其中进行开发(按产品生产流程进行开发,多用于单品种或同类型产线),企业可以根据自身情况选择。不管以何种方式开发CCS,其目标都是用以保护产品质量免受微生物、颗粒、热原/内毒素和病毒污染。表1列举了PDA TR90推荐的需进行CCS开发的详细名目。
表1:CCS开发推荐分类名目
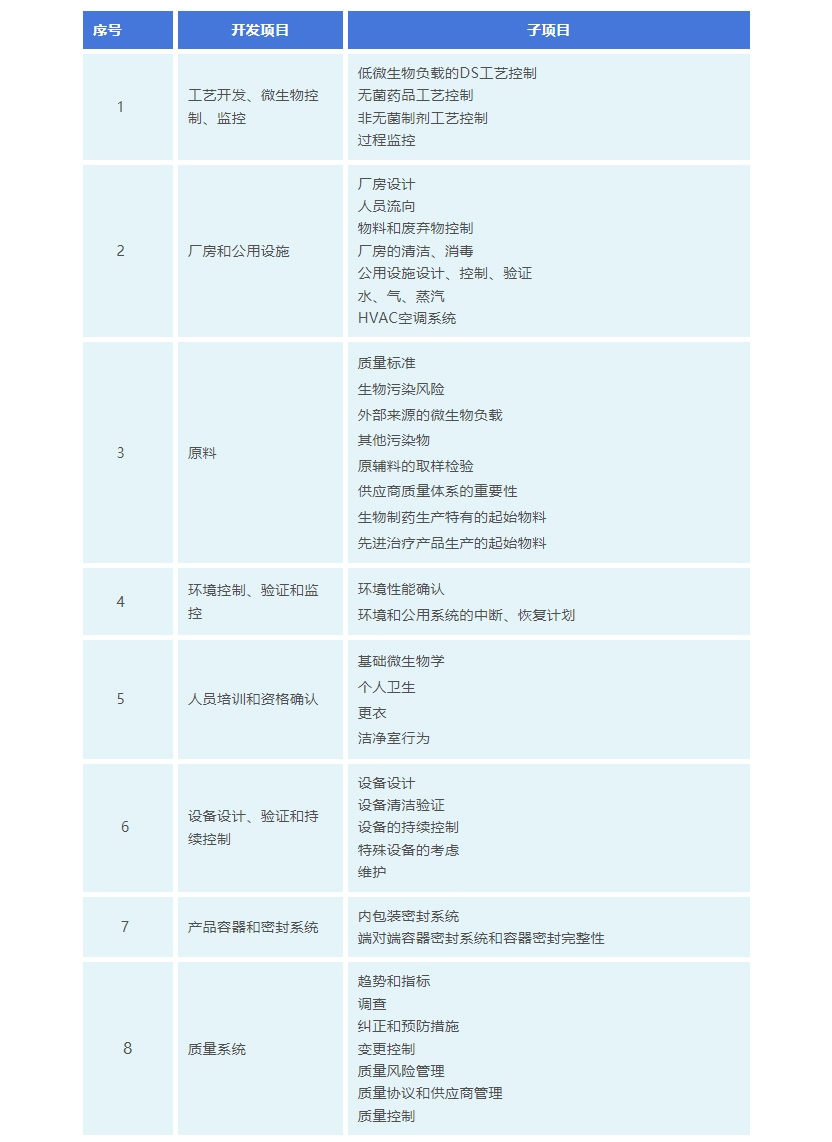
针对无菌生物药生产的全部过程,PDA TR90报告给出了表1内工艺控制考虑因素的举例,详见表2无菌生物制品工艺控制的考虑因素。

表2:无菌生物制品工艺控制的考虑因素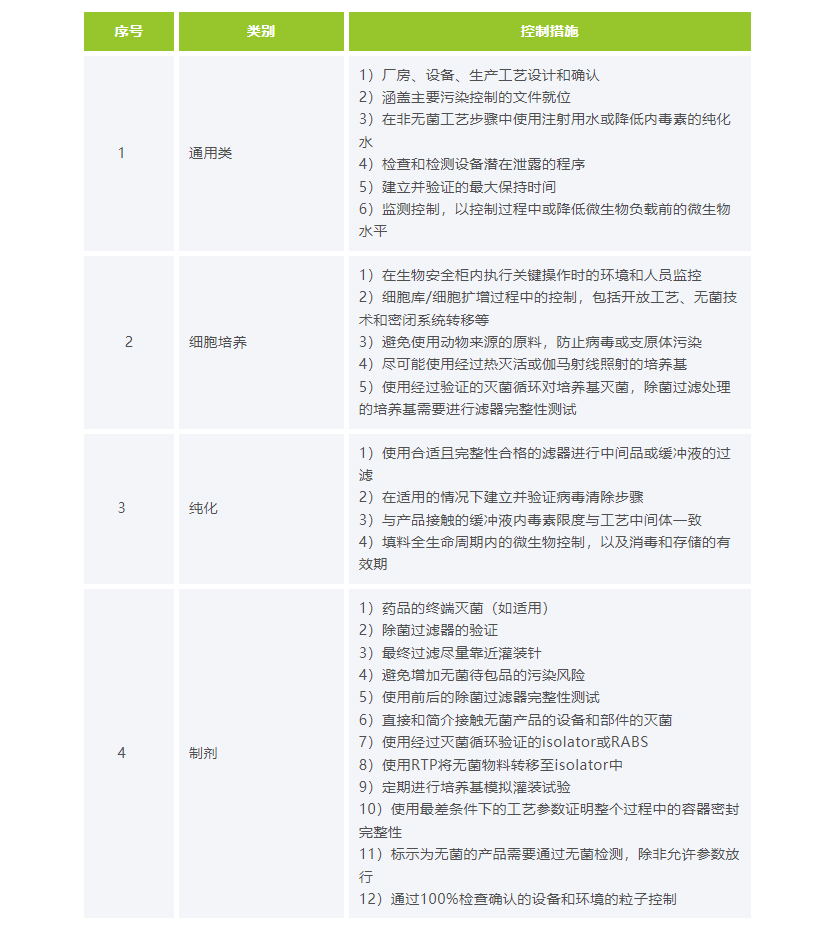
如表2所示,制剂生产中(原液阶段也需要考虑),容器密封完整性是需要控制的因素之一,而容器密封完整性正是容器密闭系统(CCS另一定义)的关键指标之一,图二展示了影响容器密封完整性的各项因素。由此可知,旧CCS定义(容器密闭系统)是新CCS定义(污染控制策略)的其中一个分支、子项,制药人再次接触单独的CCS定义时不要再发生混淆。
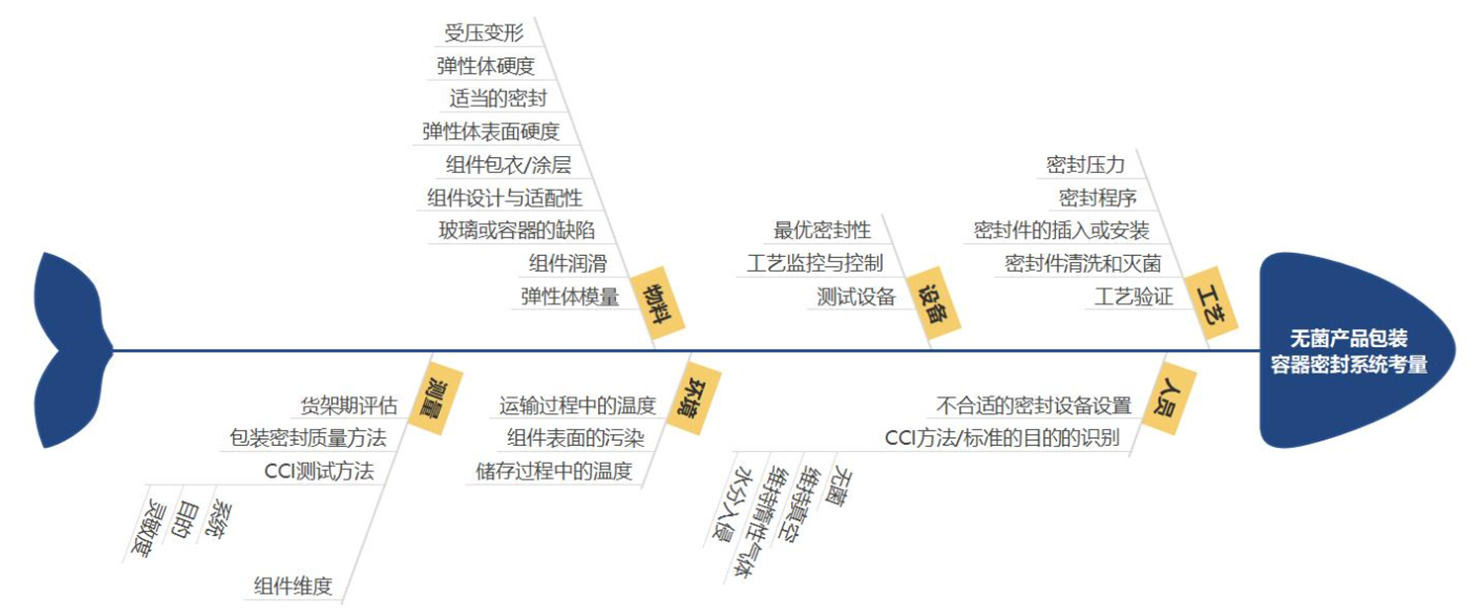
图二: 影响容器密封系统完整性的因素考量(许可转载©2018 Degrazio)
██ 小结
污染控制策略是一个系统性的工作,其方法开发需要具有各专业技能、知识的人员组成团队共同配合,远不是一个报告或一份指南所能囊括,需要各位制药人持续不断的学习、理解、持续完善。制药业内针对人员培养有培训和教育的区分,培训的目的是告诉人员如何做以及做到什么样的标准,教育的目的是告诉人员为什么要做这些,而污染控制策略就要求制药人在开发的过程中既要考虑“培训”也要兼顾“教育”,在制定标准和做法的同时也说明措施的必要性,既要“授人以鱼”也要“授人以渔”。

赋成生物制剂生产平台配有先进的进口及国产隔离器生产线,配置一次性配液灌装系统,能够满足2R、6R、10R、20R等不同规格产品的水针或冻干产品生产,欢迎各位垂询。


参考文献
1. PDA Technical Report No. 90: Contamination Control Strategy Development in Pharmaceutical Manufacturing







