
▊▊ 引言
稳定的配方是生物大分子药物成功开发的关键。成功的配方不仅能够保证临床效果,而且可以提高药物的可生产性和稳定性。生物大分子结构复杂,构象稳定性体现了其在不同条件下维持自身高级结构的能力,是决定其可开发性的关键属性之一。因此在配方开发过程中,构象稳定性成为筛选最优配方的关键指标。

差示扫描荧光法(DSF)利用环境敏感的染料(如SYPRO Orange)与蛋白质疏水区域结合后荧光强度的变化,进行构象稳定性的评估。在水溶液中游离的染料产生的信号十分微弱,可以忽略不计,但是一旦存在解折叠的蛋白质,荧光染料就可以和解折叠的蛋白质的疏水区域相结合,产生显著的荧光信号。与DSC方法相比,DSF方法具备以下特点:
4)检测时间短
除此之外,DSC对于蛋白质浓度范围通常有一定的限制, DSF则可以对0.05-200 mg/mL浓度范围内的蛋白质进行检测,而对于蛋白药物考察其在长期贮存的配方浓度条件下的稳定性是更加关键和必要的。我司利用DSF方法,对抗体类药物常用抗体配方进行了大规模的筛选考察,并利用强降解实验,研究了DSF与其他方法的相关性。
▊▊ 大规模配方筛选
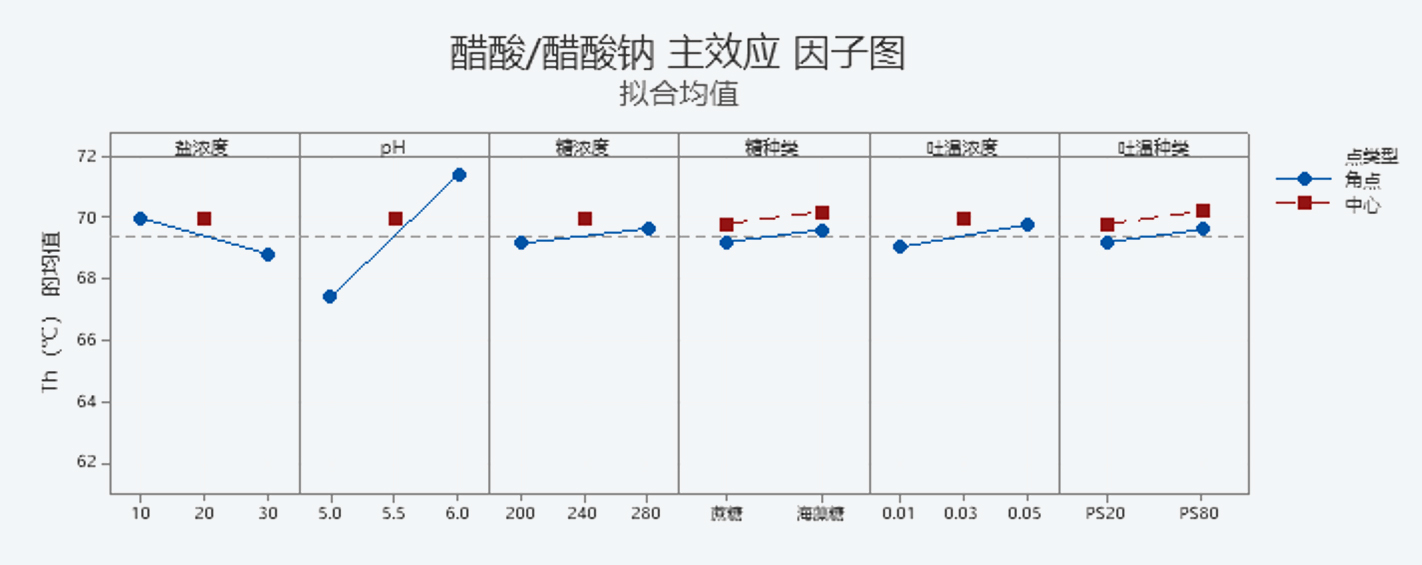
采用单克隆抗体mAb 1 (单抗,IgG 1, pI 9.1),考察表 1所示缓冲体系和辅料类型及浓度。试验设计采用DOE的方式进行,根据4种缓冲盐种类设计4组DOE试验,采用1/4析因、分辨度Ⅳ,共80组配方。全部配方采用DSF方法检测Th(蛋白质疏水暴露温度the transition temperature of exposure of the hydrophobic regions of proteins),并对检测结果进行汇总分析,如图1所示。

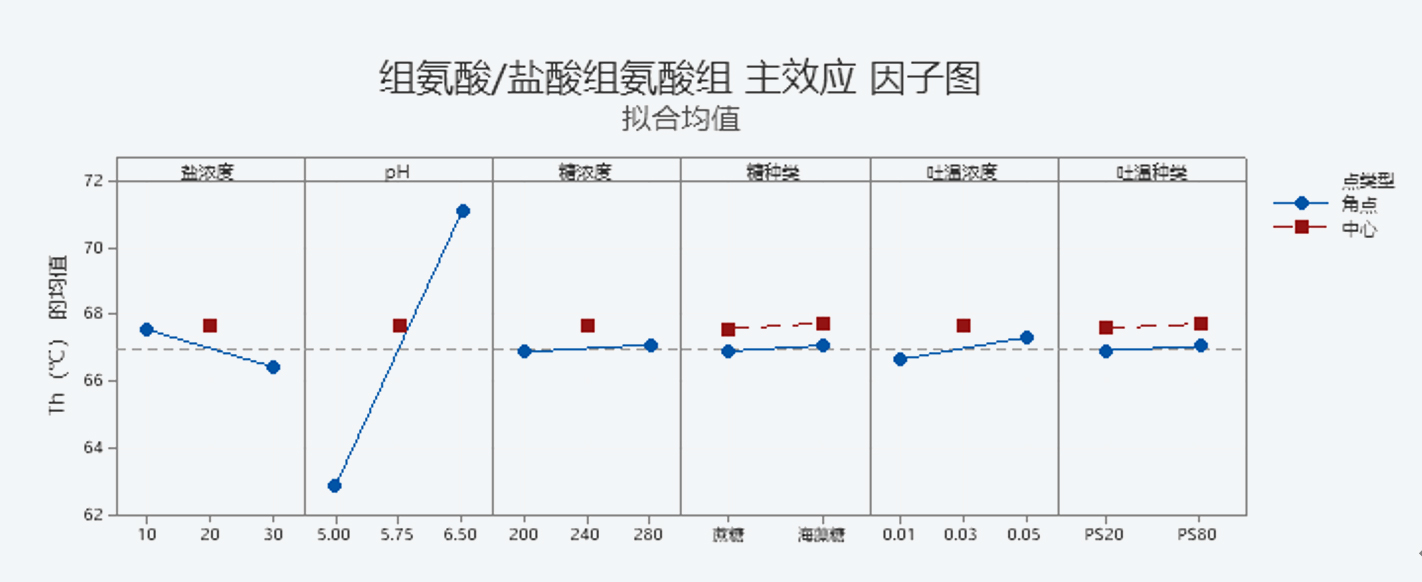
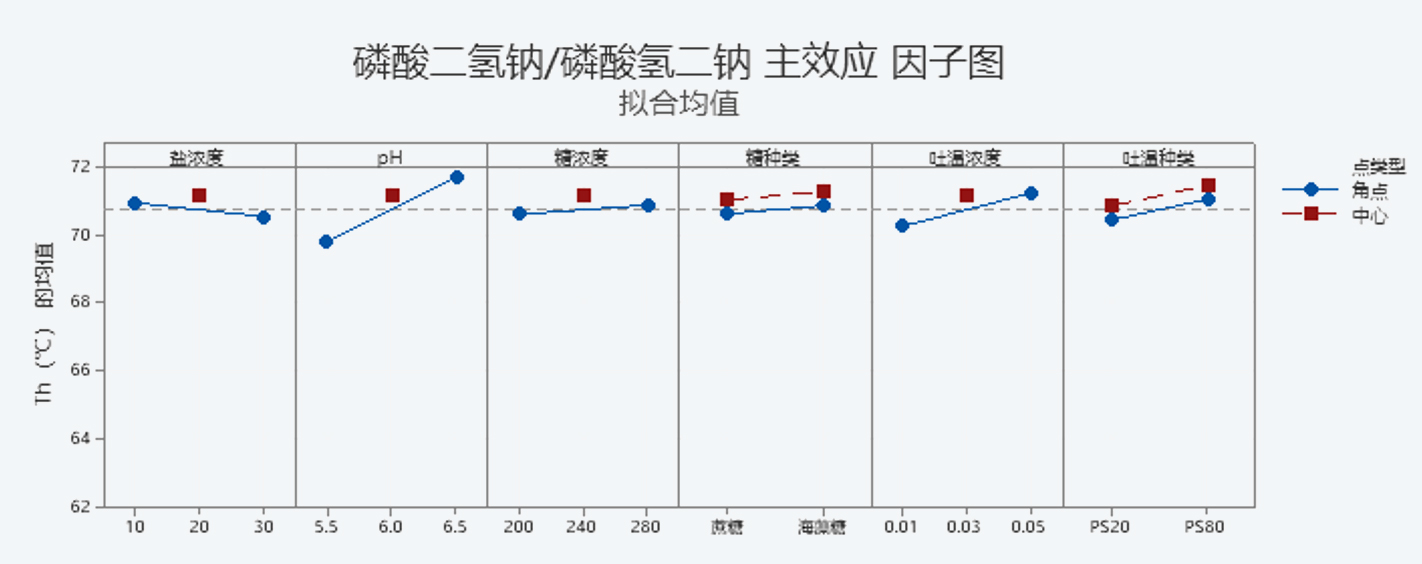
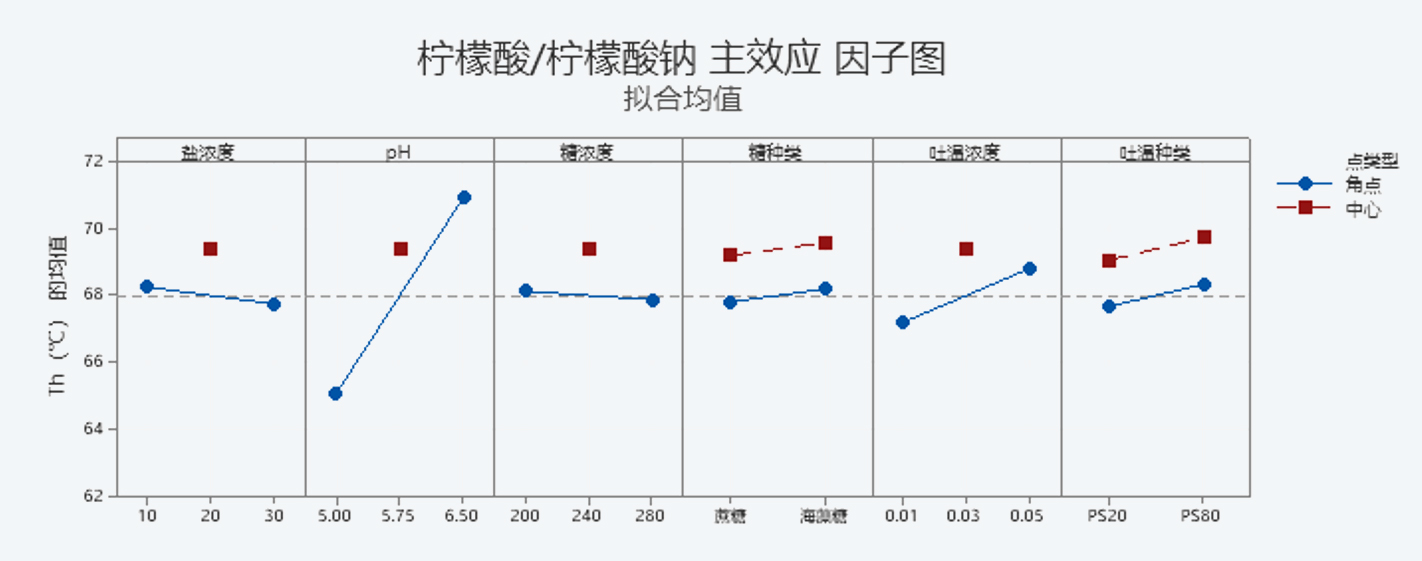
通过对主效应分析发现,在所有缓冲体系中,pH值为影响抗体Th值的最显著的因素,且Th值呈现出随着pH的增加而增加的趋势,在章节3中,我们对这种趋势进行了进一步的研究。
配方中缓冲盐浓度通常在0.01 M-0.02 M之间,最低缓冲盐浓度达到0.003 M,最高浓度可以达到0.10 M。在本次试验中考察了0.01-0.03 M缓冲盐浓度对抗体热稳定的影响,高浓度(0.03 M)的缓冲盐对抗体的热稳定性产生了不利影响,在0.02 M缓冲盐浓度下可以获得最高的Th值,此浓度也是抗体药物配方中常见的缓冲盐浓度。

表面活性剂为抗体类药物配方的重要组成部分,可以避免聚集体的产生,并且显著降低蛋白质在包装容器中储存及临床用药过程中受到的界面吸附影响。抗体配方中最常用的表面活性剂为聚山梨酯20(PS20)和聚山梨酯80(PS80),此外部分药物中添加了泊洛沙姆188 (P188),另有少量药物配方中不含表面活性剂。本次试验中考察了在含有PS20和PS80配方下的mAb 1热稳定性情况,结果显示在不同的缓冲体系下含PS80配方的抗体Th值均高于PS20的配方,其中在磷酸盐和柠檬酸盐缓冲体系中,表面活性剂种类为影响Th值的显著因素。中等浓度(0.03%)的表面活性剂对抗体的保护效果优于低浓度(0.01%)的情况,但更高浓度(0.05%)的吐温含量并不能提供更优的保护效果。

糖类是抗体药物配方中的另一个重要辅料,在冻干过程中提供网状,玻璃态、无定形的基质。目前认为糖类稳定抗体的机制包括通过水分子排除假说,玻璃化理论和降低局部及全部的流动性。在溶液中,蔗糖和海藻糖通过优先排除机制发挥作用。根据DSF结果显示,在不同缓冲体系下,蔗糖与海藻糖对Th的影响几乎相当,且中等浓度(240 mM)的糖含量更有利于抗体获得较高热稳定性。
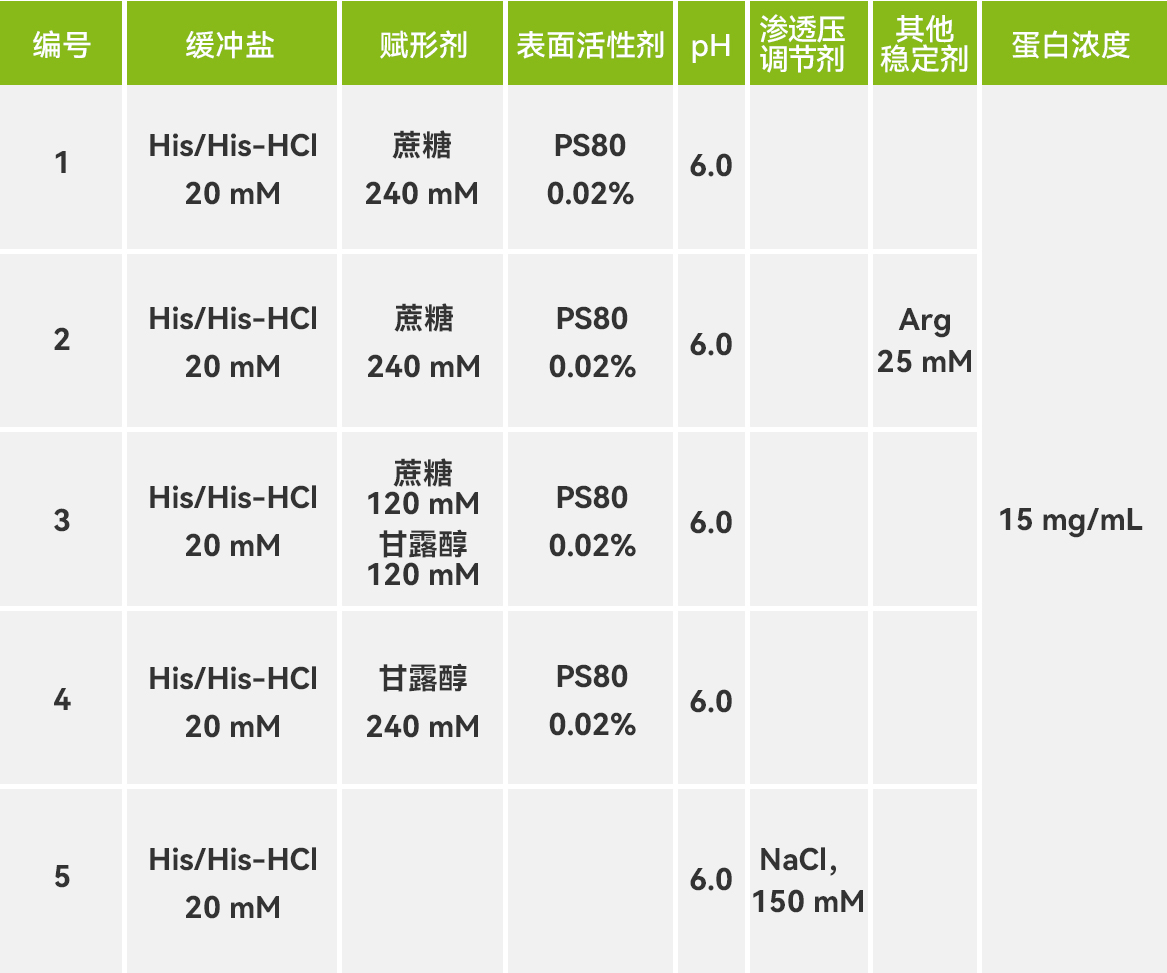
表1 配方考察内容
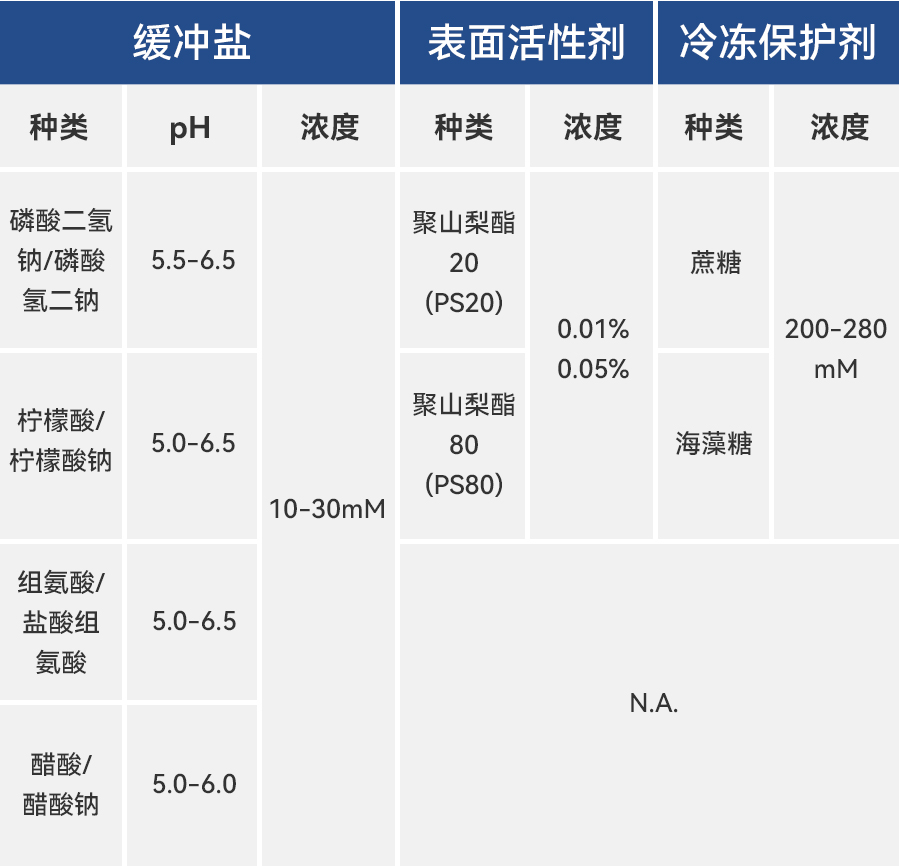
图1 四种缓冲体系的主效应因子图
▊▊ pH值对抗体Th的影响
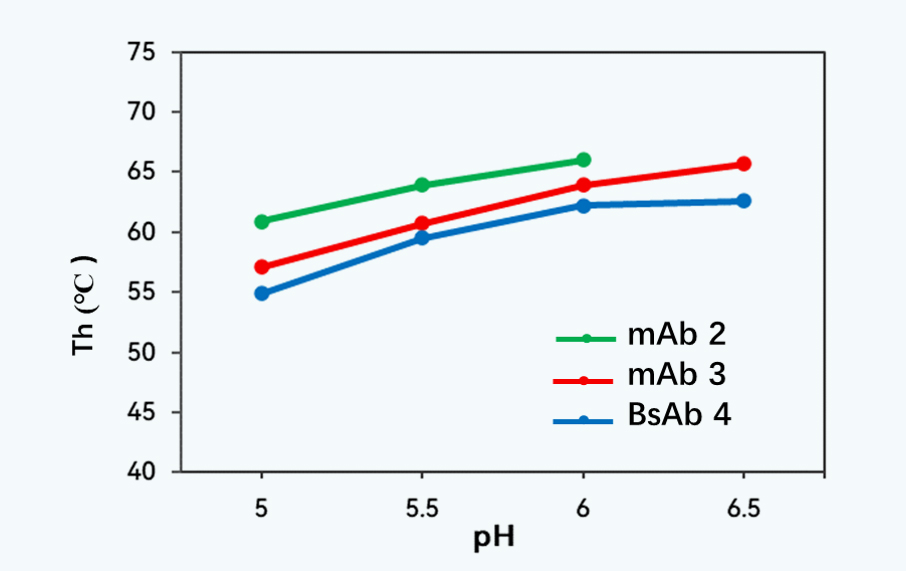
在章节2中发现在不同缓冲体系下,抗体的Th值均存在随pH的升高而上升的情况。由于配方pH的选择与抗体等电点pI相关,因此选取不同等电点的抗体mAb 2 (单抗,IgG 4, pI 6.4)、mAb 3 (单抗,IgG 4, pI 7.4)、BsAb 4 (双抗,IgG 4, pI 9.0)采用DSF进行Th的检测,如图2所示。结果显示低、中、高等电点的样品均存在Th随pH升高而上升的规律。

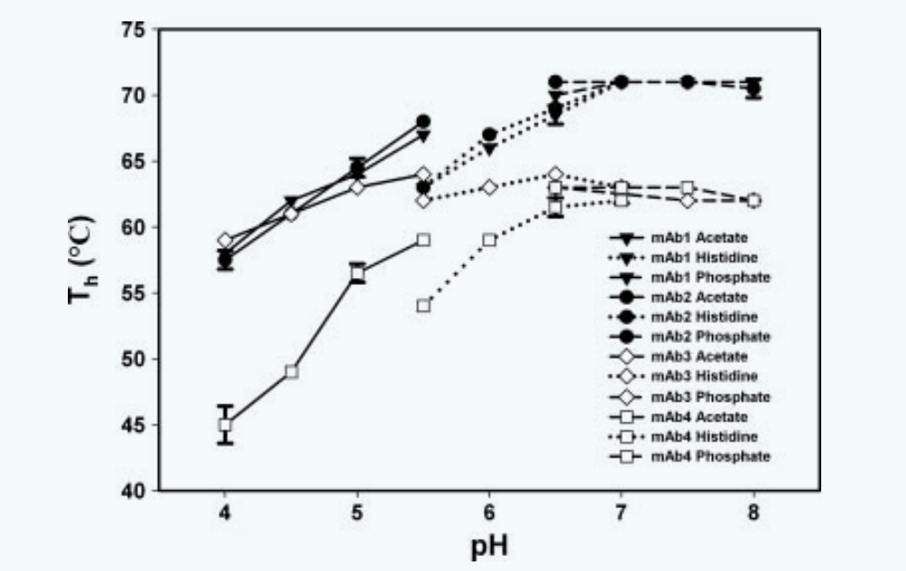
研究表明,抗体不同的结构域对热诱导和pH诱导的结构转变的敏感度不同,随着pH的降低,Fc区域首先受到影响,Fab区域在更极端的pH下才会变性。DSF主要检测的为Fc区域中CH2结构域的热稳定性变化,因此呈现出图 2和图 3所展示的规律。在低pH下的结构转变被认为是氨基酸侧链的质子化导致的,相较于自然状态结构,新生成的结构相对更为紧密,因此并不会形成更多的聚体。由于发现了这样的规律,因此DSF方法并不适宜单纯的用于含Fc结构域的抗体配方pH的筛选。
▊▊ DSF与其他方法的相关性及对产品稳定性的预测能力
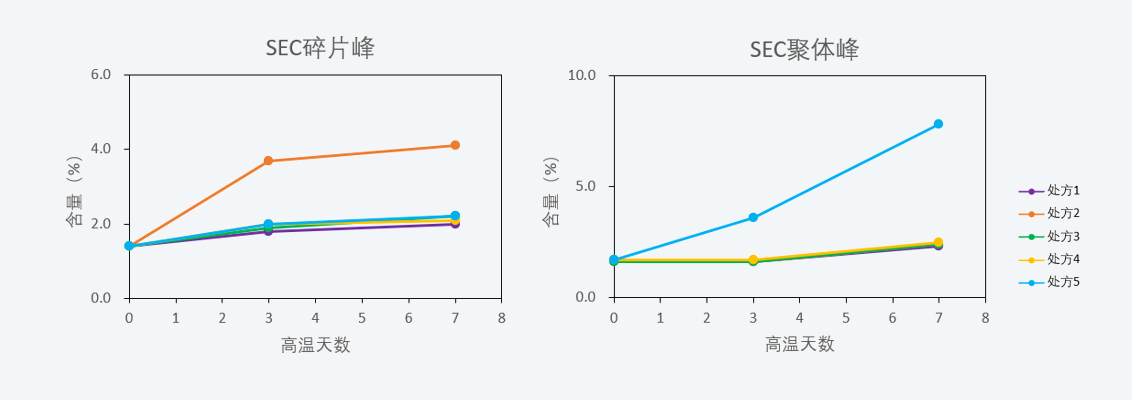
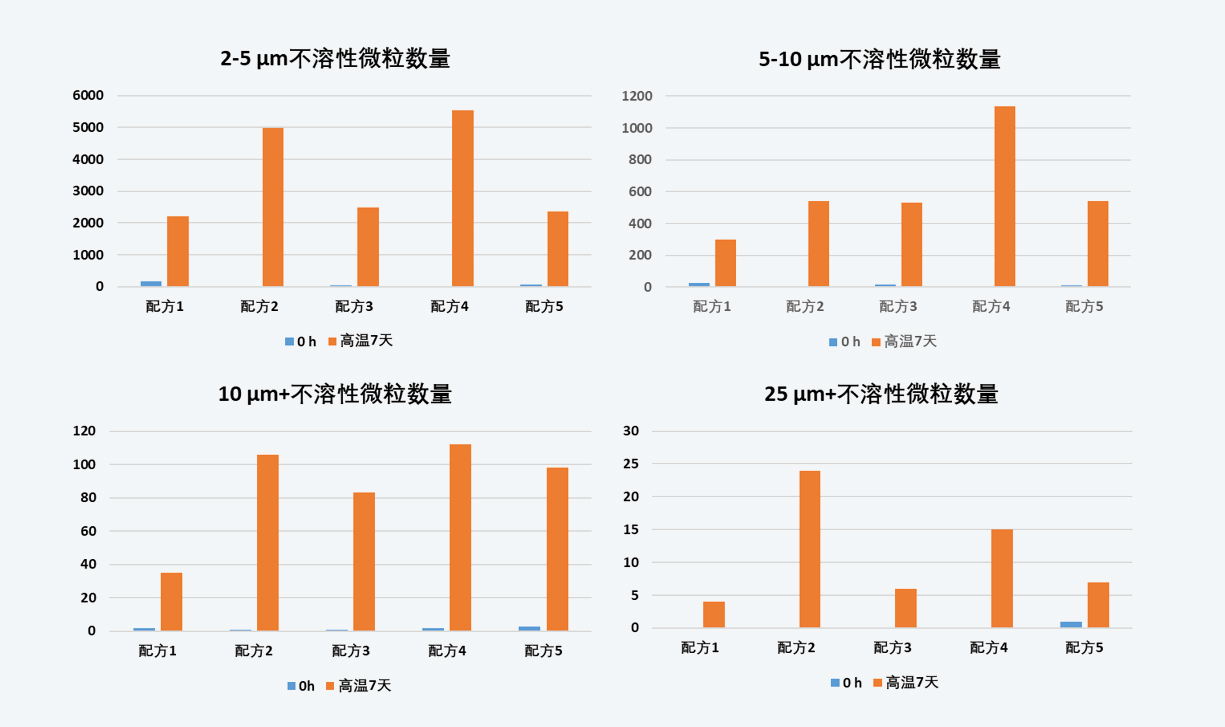
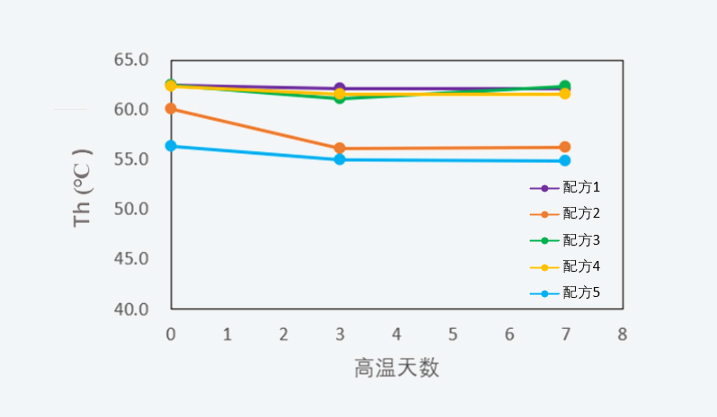
DSF利用解折叠蛋白质的疏水区域与荧光染料的结合信号来进行Th值的检测,因此DSF可以用于预测辅料对解折叠诱导的聚集体的产生的影响。聚集体含量的变化主要体现在SEC-HPLC、不溶性微粒。采用BsAb 4作为考察目标,采用单因素实验方式设计5种配方,将不同配方下的BsAb 4样品在40°C放置7天,考察样品的聚体、微粒及Th变化。表 2为单因素试验设计,图4-图6展示了40°C,7天内样品聚体、微粒及Th的变化情况。

Th结果显示配方2和配方5的热稳定性低于其他3组配方,观察SEC-HPLC和不溶性微粒检测结果,发现配方2和配方5经过高温7天处理,分别出现SEC-HPLC碎片峰和聚体峰显著升高的现象,配方2在高温7天时的不溶性微粒数量高于配方1、3、5。DSF和SEC-HPLC、不溶性微粒检测结果基本一致,表明了三者之间具有一定的相关性。随高温条件放置,初始Th较低的配方表现出较差的稳定性,说明该方法可以在一定程度上预测样品长期放置的稳定性情况。
▊▊ 总结


DSF能够在短时间内获得大量的有效数据,结合DOE的实验设计,可以在项目早期对大范围影响因素和条件进行考察,分析多种因素对蛋白质稳定性的影响情况,从而缩小配方开发的筛选范围,提高配方开发速度。同时DSF所需的仪器设备简单,生物制药实验室常见的qPCR仪即可满足检测需求,大大减少了开发所需的时间和资源,具有极高的推广利用价值。
参考文献
[1]High throughput thermostability screening of monoclonal antibody formulations[J]. Journal of Pharmaceutical Sciences, 2010, 99(4):1707-1720.







